Rozhovor o klostridii by byl neúplný bez jejího nejnemocničnějšího zástupce Clostridium difficile.
Materiály jsou určeny výhradně lékařům a specialistům s vyšším zdravotnickým vzděláním. Články mají informační a vzdělávací charakter. Samoléčba a autodiagnostika jsou extrémně nebezpečné pro zdraví. Autor článků neposkytuje lékařské rady: klinický farmakolog je lékařem pouze a výhradně pro lékaře.
Autor: Trubacheva E.S., lékař – klinický farmakolog
Rozhovor o klostridiích by byl neúplný bez jejich intranemocničního zástupce – Clostridium difficile. Nyní je navíc nejvhodnější příležitost si to připomenout, protože všechny druhy schémat, včetně antibakteriální terapie, při léčbě virové pneumonie způsobené SARS-CoV-2 v nemocnicích se změněným účelem by mohly dále trénovat nozokomiální mikroflóru, která zahrnuje výše uvedené klostridium.
V současné době toxigenní kmeny C.tuhý jsou považovány za jasného původce nozokomiálních infekcí. To znamená, že pseudomembranózní kolitida, kterou způsobují, je onemocnění spojené s poskytováním lékařské péče, tedy iatrogenní. A všichni víme, jak to vyšetřovací výbor vnímá a hlavně nehodlá přestat (podle posledního rozhovoru s předsedou vyšetřovacího výboru A. Bastrykinem). Proto je nutné co nejpodrobněji porozumět tomu, jak je tato nemoc způsobena, co ji vyvolává a jak, pokud se jí nevyhnete, pak ji co nejúčinněji léčit. O tom bude aktuální rozhovor.
Mikrobiologické aspekty
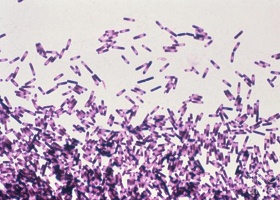
C.tuhý, stejně jako ostatní klinicky významné klostridie, je striktní anaerob. Hlavním škodlivým faktorem pro ni, stejně jako pro ostatní klostridie, jsou toxiny, a stejně jako ostatní klostridie, C.tuhý ví, jak vytvářet spory. Nemoc způsobená toxigenní C.tuhý, tzv. pseudomembranózní kolitida.
Nyní si povšimněme některých podrobností:
- C.tuhý jsou v přírodě rozšířené – v přírodních nádržích, půdě, koupalištích, ale nemají schopnost produkovat toxiny, a proto nemají klinický význam.
- У C.tuhý Existují přirození antagonisté, kteří dokážou potlačit její nekontrolovanou reprodukci v tlustém střevě a také to dělají. Mezi takové antagonisty patří enterokoky, laktobacily, bifidobakterie, nesporogenní anaeroby a – náhle – Pseudomonas aeruginosa. Dokud je tato flóra neporušená, žádný problém C.tuhý nedoručí.
- Pokud antagonisté z nějakého důvodu zemřeli nebo se jejich počet prudce snížil, pak C.tuhý získává selektivní výhodu a kromě rychlého rozmnožování začíná neméně rychlá tvorba toxinů. Ke klinicky významným toxinům C.tuhý zahrnují enterotoxin A a cytotoxin B, které patří do rodiny „hlavních klostridiových toxinů“. Navíc je třeba mít na paměti, že toxiny fungují výhradně ve dvojicích a C.tuhý, který jich nemá plnou sadu, nemůže způsobit klasickou pseudomembranózní kolitidu (PMC).
- Samostatně stojí za zmínku fenomén, který se týká novorozenců a dětí mladších jednoho roku. Ve střevech se nachází až 70 % zcela zdravých dětí C.tuhý, navíc produkující toxin A a přitom nezpůsobující absolutně žádné klinické příznaky, i když se jim někdy snaží přisoudit „náhlou smrt novorozenců“. Dokud však neexistuje žádná klinika, měl by být tento jev považován za zdravé přenášení, zejména proto, že na konci prvního roku života klesne úroveň přepravy na 9% a poté se stane stejným jako u dospělé populace – ne více než 3 %. Proč se nemoc nerozvíjí? Předpokládá se, že je to způsobeno nezralostí střevního receptorového aparátu, který jednoduše „nevidí“ toxin, a proto nereaguje.
Epidemiologické aspekty
Hlavní zdroj toxigenních látek C.tuhý je buď pacient, nebo zdravý přenašeč. Cesta šíření je fekálně-orální nebo kontaktní. Od té kontroverze C.tuhý bezpečně přetrvávají až 180 dní, některá ohniska se mohou objevit bez zjevně identifikovatelného zdroje – spíše špatně vyčištěné nemocniční toalety, stejně jako dlouhodobě či nesprávně ošetřované matrace. Pokud by se navíc na oddělení náhle vyskytl asymptomatický nosič C.tuhý z řad zdravotnického personálu a zbytek není nijak zvlášť zvyklý si mýt ruce, pak každý druhý zaměstnanec bude tyto spory šířit nikoli oddělení, ale celé nemocnice – na ruce, pláště, chytré telefony, posazovat je na stoly, zábradlí a klávesnice, samy o sobě zcela asymptomatické, ale s katastrofálními následky pro pacienty.
Proč nemocnice? Protože zde se používá největší počet antibakteriálních léků, včetně ne vždy oprávněných a C.tuhý může získat selektivní výhodu v důsledku snížení počtu antagonistických bakterií, které dříve omezovaly jejich reprodukci a uvolňování toxinů.
V jakých odděleních Jsou nejčastěji možné případy (nebo dokonce celá ohniska) pseudomebranózní kolitidy?
- Jednotky intenzivní péče z důvodu maximálního využití antibakteriální terapie
- Chirurgická oddělení téměř jakéhokoli profilu
- Popálit oddělení
- Onkologická oddělení užívající chemoterapeutika
Pokud byl tedy váš pacient v nedávné minulosti z jakéhokoli důvodu na jednom z těchto oddělení, musíte mít na paměti riziko možného přenosu toxigenních C.tuhý a vývoj MVP v případě antibiotik.
Která antibiotika nejčastěji vyvolávají zvýšení počtu toskogenních C.tuhý a rozvoj pseudomembranózní kolitidy?
- Vysoké riziko vykazuje klindamycin, cefalosporiny třetí generace (nejnebezpečnější je ceftriaxon, zejména ve vysokých dávkách), fluorochinolony
- Střední riziko je pozorováno při použití penicilinů a úzkospektrálních cefalosporinů (jako je ceftazidim), karbapenemů, makrolidů, kotrimoxazolu
- Metronidazol, tetracykliny, vankomycin, aminoglykosidy mají nízké riziko
- Při užívání sulfonamidů, nitrofurantoinu a fosfomycinu nehrozí žádné riziko
Jednoduše řečeno, co vyrazí hlavní konkurenty z tlustého střeva C.tuhý, pak poskytuje vysoké riziko rozvoje MVP. Kromě antibiotik však MVP vyvolávají také cytostatika, jako jsou například platinové léky a methotrexát.
Kteří pacienti jsou vystaveni riziku nákazy toxigenním patogenem? C.tuhý a vývoj PMK? Nejčastěji se jedná o zpočátku těžké pacienty s popáleninami, po operaci tlustého střeva, pacienty se selháním ledvin a případné pacienty na jednotkách intenzivní péče. A z nějakého důvodu pacienti s HIV vykazují statistiky podobné běžné populaci – nic více a nic méně.
Na základě všeho, co bylo řečeno, hlavní věc v obsahu C.tuhý je prevence, jejímž základním kamenem je epidemiologický dozor. Pouze naprostá čistota rukou a toalet, jak pro pacienty, tak pro personál, a také důsledné dodržování požadavků SanPin, zejména ve zdravotnických zařízeních, které se s touto šelmou již setkaly, mohou zabránit novým případům. Dovolte mi připomenout, že úmrtnost na pseudomembranózní kolitidu je více než 50% a na rozvinuté toxické megakolon je 100%.
Klinické aspekty
Hlavní problém spojený s C.tuhý, je její diagnóza. Na jedné straně je vše jednoduché – již dlouho existují komerční testovací systémy, které umožňují rychlým testům detekovat toxiny, na druhé – no, upřímně, kdo je kdy viděl osobně? Za 15 let práce to autor nikdy neviděl. Mikrobiologická diagnostika vyžaduje přítomnost v laboratoři nejen anaerobního analyzátoru, ale také speciálně vyškoleného bakteriologa. A kde můžeme získat všechen tento luxus? Praktický lékař tedy musí stanovit diagnózu na základě klinických projevů, přičemž nezapomene ani na diferenciální diagnostiku s dalšími možnými infekčními onemocněními tlustého a tenkého střeva (o kterých jsme již psali v dřívějších článcích: viz zde, zde a zde). Navíc je potřeba myslet na nemocniční střevní infekce, které taky nikdo nezrušil (i když jsem je už dlouho neviděl).
Zároveň si musíte pamatovat na průjem spojený s antibiotiky, který nemá nic společného s MVP a C.tuhý nemají a vysvětlují pouze farmakodynamiku předepsaných léků. Například průjem spojený s užíváním amoxicilinu/klavulanátu je způsoben tím, že jeho metabolity stimulují motilitu tlustého střeva, nebo makrolidy působí na motilinové receptory a způsobují úplně stejný průjem. A když se tyto dva léky předepisují v kombinaci, jak to rádi dělají v ambulantní praxi, pak se průjmy spojené s antibiotiky nebudou objevovat jen u těch nejodolnějších pacientů. Mimochodem, pokud pacienty stále nevarujete před tímto extrémně laxativním účinkem, pak začněte. Ale opakujeme, aby C.tuhý To vše je zcela irelevantní. Téměř vždy se ambulantní stavy řeší nahrazením léku něčím méně agresivním na střeva a revizí souběžné terapie (např. mohou být i NSA, která mohou také vyvolat průjem).
Co je průjem způsobený infekcí? C.tuhý odlišná od všeho ostatního? Jasná souvislost s hospitalizací a zahájením užívání antibiotik, zvláště pokud byl pacient pár měsíců předtím, než se nám dostal do rukou, hospitalizován na dříve indikovaných odděleních. Pokud se u takového pacienta třetí den po předepsání např. ceftriaxonu objeví průjem, měl by okamžitě zazvonit poplašný zvonek. Máte-li přístup k rychlým testům, zjistěte přítomnost toxinů, pokud ne, okamžitě vysaďte antibiotika. Pokud stále existuje potřeba antibakteriální terapie, změňte ji na lék ze seznamu bezpečných. Beta-laktamy by se neměly předepisovat! Žádný! Dokud nezjistíme, co se s pacientem děje. Sám pacient v této době (den, maximálně dva) musí být velmi pečlivě sledován a v žádném případě by mu neměl předepisovat žádné léky snižující střevní motilitu.
Pokud se změnou antibakteriálního léku na stavu pacienta nic nezměnilo, zvyšuje se i počet epizod průjmu nebo se začíná prohmatávat napjaté tlusté střevo, pak lze hovořit o pseudomembranózní kolitidě, kterou lze potvrdit endoskopickými metodami, kde závěr bude indikovat přítomnost charakteristických pseudomembrán v určitých oblastech nebo celé délce tlustého střeva přístupné pro kontrolu.
Co a jak léčit?
- Jednak takový pacient potřebuje izolaci, jinak znovu nakazí všechny kolem sebe.
- Za druhé, vše závisí na závažnosti příznaků, pro mírné a středně těžké používáme perorální metronidazol (potřebujeme dodat lék do střevního lumen), pro těžké – vankomycin a také perorálně, hlavní věc je, že neexistuje žádný toxický megakolon, protože v tomto případě pacient zůstává maximálně XNUMX hodin a smrtelný výsledek v tomto stavu je stoprocentní
Jaká je výhoda metronidazolu? Nezpůsobuje selekci rezistentních kmenů enterokoků (o enterokocích jsme hovořili zde), je dostupnější a je několikanásobně levnější než i nejlevnější vankomycin. Zároveň se díky jeho nekontrolovanému používání již vytvořila poměrně slušná zásoba kmenů pro jakýkoli případ průjmu C.obtížné rezistentní vůči němu, takže metronidazol by neměl být předepisován pacientům, kteří již měli epizody nozokomiálního průjmu léčeného, protože není pravda, že nebudete čelit pacientovi, který již prodělal epizodu MVP, vegetativní C.tuhý vyřazeny a spory stabilních forem nyní čekají v křídlech.
Závěrem podotýkáme, že nemocnice, které byly bývalými „covidárii“, se nyní začaly vracet do provozu, ve kterém využívaly, co se dalo, a zaměstnanci si po dlouhých měsících pobytu ve zvláštní ochraně najednou mohou odpočinout v dodržování hygienických zásad. a epidemiologická pravidla, a právě proto jsme připomněli o C. difficile, která jako časovaná bomba dokáže vybuchnout tam, kde to bylo zcela nečekané. Proto je lepší nepolevovat.

Clostridium (clostridium spp) je infekční onemocnění s akutním průběhem. Nechává se vyprovokovat klostridie – Gram-pozitivní anaerobní bakterie, které mohou produkovat endospory. Díky tomu jsou dobře zachovány ve vnějším prostředí. Právě odrůdy těchto bakterií produkují nejtoxičtější jedy: botulotoxin, tetanospasmin, ε-toxin. Způsobují velmi závažná onemocnění: tetanus, botulismus, plynová gangréna atd. Nejčastěji ale k infekci dochází bakterií Clostridium difficile. Normálně jsou tyto bakterie součástí mikroflóry gastrointestinálního traktu a genitálního traktu u žen. Clostridium difficile je zástupcem normální mikroflóry, příčiny kolitida a enterokolitida s příliš aktivní reprodukcí. Toxin produkovaný bakteriemi Clostridium perfringens, může vyvolat otravu jídlem a toxin, který se tvoří clostridium botulinum, způsobuje botulismus.
Patogeneze
- Clostridium difficile jsou grampozitivní tyčinky, které produkují dva exotoxiny: enterotoxin A a cytotoxin B. Oba vyvolávají průjmový syndrom. Clostridium difficile ve formě spor vykazuje vysokou odolnost ve vnějším prostředí a může přežívat ve střevě i při vysokých koncentracích řady antibiotika. Clostridia difficile je hlavním původcem pseudomembranózní kolitidy, nebezpečného stavu pro novorozence a malé děti. Navíc vyvolávají další enterokolitidu a kolitidu po iracionální antibiotické léčbě. Patogen se přenáší kontaktem. Onemocnění způsobené tímto patogenem se vyvíjí během léčby širokospektrými antibiotiky nebo po ní. Pod vlivem některých antibakteriálních léků (např.linkomycin, clindamycin, ampicilin atd.) dochází ke změnám střevní mikroflóry a objevují se kolonie Clostridium difficile. Aktivně se rozmnožují a vyvolávají onemocnění. Onemocnění se také může vyvinout v důsledku exogenní infekce během nebo bezprostředně po antibakteriální léčbě. Onemocnění se rozvine ihned po přerušení léčby nebo po několika týdnech, může být vleklé nebo se stát chronickým.
- Clostridium perfringens – grampozitivní bakterie, původci toxických infekcí a plynaté sněti. Clostridium perfringens je zástupcem oportunní mikroflóry, dlouhodobě přetrvávají ve vnějším prostředí. Bakterie Clostridium perfringens způsobuje alimentární onemocnění. A když se Clostridium perfringens dostane do otevřené rány, produkují toxiny, které poškozují okolní tkáně a vytvářejí podmínky pro další šíření infekce. C. perfringens typ A je hlavním etiologickým faktorem plynaté gangrény.
- Clostridium botulinum – anaerobní bakterie, která se vyvíjí v nepřítomnosti kyslíku. Produkuje spory, které jsou široce distribuovány v půdě, vodě atd. Bakterie vstupují do potravin, rostou v nich a produkují toxiny. Po konzumaci kontaminovaných potravin, hlavně konzerv, se člověk nakazí botulismem.
- Clostridium tetani – grampozitivní anaerobní bakterie, která tvoří spory. Je to původce tetanu. Přenášeno kontaktem. Bakterie produkují tetanospasminovlivňující nervový systém a vyvolávající tonické kontrakce příčně pruhovaných svalů. Je neutralizován antitetanovým sérem. Bakterie také produkuje tetanolysin.
Klasifikace
K dnešnímu dni bylo identifikováno více než sto druhů klostridií. V medicíně je jejich klasifikace založena na několika principech. Podle morfologie se rozlišují tyto skupiny:
- tyčinky s kulatou, koncovou výtrusem (C. tetani);
- tyčinky s oválnou subterminální sporou (C. botulinum);
- se subterminální nebo centrálně umístěnou oválnou sporou (původci plynové gangrény).
Podle typu patologických procesů:
- enterální klostridiózy (C. botulinum, C. perfringens, C. difficile);
- traumatické a posttraumatické (C. tetani, C. perfringens, C. novyi, C. histolyticum, C. septicum);
- generalizované infekce: septikémie, sepse.
Příčiny
Normálně jsou klostridie přítomny ve střevní mikroflóře u dospělých a dětí. Clostridia ve stolici dospělého by neměla překročit 105 CFU/g. Pokud jsou však aktivovány, a proto se množí příliš rychle, vede to ke zhoršení pohody a rozvoji onemocnění. Aktivace těchto bakterií může být vyvolána některými vnějšími a vnitřními faktory:
- Konzumace nekvalitních potravin – sešívané, nekvalitní, zkažené výrobky, dále rychlé občerstvení a další nezdravé potraviny.
- Pravidelné stresové situace.
- Nepříznivé podmínky prostředí.
- Neustálý nedostatek spánku nespavost.
- Oslabený imunita.
- Užívání antibiotik, hormonálních léků, imunosupresiv.
- Infekce střev.
- Nezralost centrálního nervového systému.
- Časté nachlazení chřipka.
- Chirurgie
Příznaky
Klostridióza nemá typický klinický obraz. Projevy závisí na tom, v jakém systému patologický proces začal. Stále však existuje několik příznaků, které se objevují bez ohledu na typ patogenu:
- Zvýšená tělesná teplota – může dosáhnout 39 stupňů.
- Vzhled ostré bolesti břicha spastické povahy. Když se provádí palpace, bolest se stává výraznější, stěny břišní dutiny se napínají.
- Plynatost, nadýmání.
- Hubnutí v důsledku nedostatku chuti k jídlu a zhoršení zdraví.
- Průjem, krev a části potravy jsou někdy detekovány v tekutých výkalech.
- Nevolnost, časté zvracení, někdy přítomnost krve ve zvratcích.
Clostridiosis difficile se vyvíjí jako pseudomembranózní kolitida, ve vzácnějších případech – průjmový syndrom nebo nekrotizující enterokolitida.
Jako typ pseudomembranózní kolitidy se onemocnění nejčastěji rozvíjí u novorozenců a kojenců. Onemocnění začíná akutně – stoupá tělesná teplota, dítě plive, zvrací, vzniká průjmový syndrom. Vodnatá stolice obsahuje hlen a někdy krev. Často dítě vyprazdňuje hustý hlen s vláknitými skvrnami. Stolice může být i hnisavá. Kůže získává šedo-bledou barvu a na břiše je viditelná síť žil. Děti pociťují nadýmání a odmítají jíst. V souladu s tím děti hubnou. Je možné vyvinout krvácení ve střevech, což je extrémně život ohrožující stav.
Onemocnění je závažné u novorozenců, zejména u předčasně narozených dětí. Bez řádné léčby je možná smrt.
Analýzy a diagnostika

Pro stanovení diagnózy musí odborník prostudovat anamnézu pacienta a věnovat pozornost tomu, zda byla provedena antibiotická terapie.
Pro kontrolu přítomnosti Clostridium difficile a jejich toxinů je nutný laboratorní test stolice. V případě potřeby se provádí endoskopické vyšetření tlustého střeva, které odhalí charakteristické znaky – nažloutlé plaky na sliznici, silná vrstva překryvů, ulcerované oblasti, které mohou být důležité v procesu diferenciální diagnostiky. Může být provedena radiografie.
Provádí se také krevní test, ve kterém jsou zaznamenány nespecifické změny v manifestních formách infekce.
Léčba
Po potvrzení diagnózy se v závislosti na typu infekce provádí léčba klostridií ve stolici. Pokud se zjistí, že pacient je asymptomatický nosič Cl. obtížné, léčba se nepraktikuje.




