Mezi organickými látkami mají buňky nejrozmanitější vlastnosti a vykonávané funkce. proteiny Nebo proteinů . Bílkoviny na rozdíl od sacharidů a lipidů obsahují kromě uhlíku, kyslíku a vodíku také dusík a mohou obsahovat i atomy síry, fosforu a železa.
Proteiny jsou biopolymery, jejichž monomery jsou aminokyselin . (20) α-aminokyseliny se podílejí na tvorbě celé řady proteinů. Molekuly aminokyselin mají dvě funkční skupiny: karboxylovou (kyselou) a aminovou (zásaditou).

Aminoskupina a karboxylová skupina jsou schopny vzájemné interakce s eliminací vody a vytvořením peptidové vazby CO – NH. Peptidové vazby spojují molekuly aminokyselin dohromady a vytvářejí dlouhé řetězce. Počet aminokyselinových zbytků v řetězci může být několik stovek nebo dokonce tisíců. Takové velké molekuly se nazývají makromolekuly.
Pořadí, ve kterém jsou aminokyseliny kombinovány v makromolekule proteinu, se nazývá primární struktura. Tato struktura je jedinečná pro každý typ proteinu. Určuje struktury vyšších úrovní, vlastnosti proteinu a jeho funkce.
Polypeptidový řetězec je složen do spirály v důsledku tvorby vodíkových vazeb mezi skupinami atomů – NH a – CO, umístěnými v různých částech makromolekuly. Tato spirála se nazývá sekundární struktura proteinu.
Terciární struktura proteinu dochází při interakci aminokyselinových radikálů, stejně jako v důsledku disulfidových můstků, vodíkových a iontových vazeb. Molekula proteinu dostává tvar globule (míč).
Tvoří se některé bílkoviny kvartérní struktura. Jedná se o komplex několika makromolekul s terciární strukturou. Kvartérní struktura je držena na místě slabými iontovými a vodíkovými vazbami a také hydrofobními interakcemi.

Proteiny se mohou kombinovat se sacharidy, tuky a nukleovými kyselinami za vzniku komplexních sloučenin: glykoproteiny, lipoproteiny, nukleoproteiny.
Pod vlivem vnějších faktorů: ozáření, zahřívání, některé chemikálie atd. dochází k narušení prostorové struktury molekul bílkovin. Tento proces se nazývá denaturace.
Nejprve dochází k destrukci kvartérní struktury, poté terciární a sekundární. Při denaturaci je primární struktura zachována, ale protein ztrácí své vlastnosti a funkce.

Destrukce primární struktury je nevratná. Dochází k němu při hydrolýze bílkovin – makromolekuly se rozpadají na jednotlivé aminokyseliny. K tomuto procesu dochází v trávicích orgánech zvířat a v lysozomech buněk pod vlivem hydrolytických enzymů.
1. Nejdůležitější funkcí bílkovin je katalytickýNebo enzymatické. Enzymové proteiny se účastní všech biochemických reakcí probíhajících v buňce a mnohonásobně zvyšují rychlost těchto reakcí. Pro každou reakci existuje speciální enzym.
2. Proteiny ano konstrukční (stavební) funkce. Jsou součástí plazmatických membrán, tvoří pojivové tkáně (elastin a kolagen), vlasy a nehty (keratin).

3. Funkce signálu také prováděny proteiny uloženými v membráně. Tyto proteiny pod vlivem vnějších faktorů mění terciární strukturu, což ovlivňuje fungování buňky.
4. Transportní funkce proteiny se projevují transportem iontů přes buněčné membrány, transportem kyslíku a oxidu uhličitého hemoglobinem v krvi, transportem mastných kyselin plazmatickými albuminy atp.
5 Dfunkce motoru poskytují proteiny aktinu a myosinu, které se mohou stahovat a natahovat. Pohybují řasinkami a bičíky jednobuněčných organismů a stahují svaly u zvířat.

6. Ochranná funkce je zajišťována protilátkami imunitního systému těla, proteiny systému srážení krve (fibrinogen, protrombin aj.).
7. Regulační funkce provádět hormonální proteiny (inzulín, thyrotropin, somatotropin, glukagon atd.).
8. Energetická funkce bílkoviny se provádějí po vyčerpání zásob sacharidů a tuků. Při úplném rozložení (1) g bílkovin na konečné produkty se uvolní (17,6) kJ energie.

Genetické informace o struktuře a funkcích všech bílkovin v těle se k nám předávají od našich rodičů pomocí speciálních bílkovin. Kromě toho tyto látky určují strukturu a tvar buňky, zajišťují rozpoznávání a vazbu různých molekul a také katalýzu a regulaci chemických reakcí probíhajících v našem těle. A to je stále neúplný výčet funkcí bílkovin v lidském těle!
· Aktualizováno 25. října 2022
Co jsou proteiny
Proteiny – Jedná se o vysokomolekulární organické sloučeniny, které se skládají z aminokyselinových zbytků spojených navzájem peptidovými vazbami.
Tuto třídu organických látek lze posuzovat z hlediska dvou věd: biologie a chemie. Začněme biologickou úlohou bílkovin.

Biologické funkce bílkovin
Konstrukce nebo plast
Proteiny jsou základem stavebního materiálu všech buněčných membrán, protože tvoří základ protoplazmy každé živé buňky. Určitě znáte proteiny jako kolagen, keratin a elastin. Tvoří základ pojivové tkáně těla a zajišťují její pevnost.
Doprava
Tato funkce spočívá v navázání chemických prvků nebo biologicky aktivních látek, tedy hormonů, a jejich přesunu do různých tkání a orgánů těla. Například hemoglobin je přenašečem kyslíku v krvi a podílí se také na transportu oxidu uhličitého. K přenosu nasycených mastných kyselin v krvi do celého těla dochází za účasti albuminu. Transferin transportuje ionty železa a speciální proteiny se podílejí na transportu iontů sodíku a draslíku přes buněčnou membránu.
Regulační
Proteiny hrají roli v regulaci a koordinaci metabolismu v různých buňkách těla. Inzulin například reguluje hladinu glukózy v krvi a také zvyšuje tvorbu tuků ze sacharidů.
Ochranný
Když cizí protein nebo mikroorganismus vstoupí do těla, vytvoří se speciální proteiny – protilátky. Obranou organismu proti nadměrné ztrátě krve je přeměna bílkoviny fibrinogen. Na tomto procesu se samozřejmě podílejí i další proteiny, jako je trombin, a také mnoho dalších srážecích faktorů. Ochranu našeho žaludku před vlivy silně kyselého prostředí zajišťuje bílkovina mucin, základem pokožky je kolagen, keratin je bílkovina ochranného vlasu.
Motor
Motorickou funkci zajišťují speciální kontraktilní proteiny, jako je aktin a myosin, které se podílejí na kontrakci kosterních svalů.
Signál
Na povrchu buněčné membrány jsou zabudovány receptory (molekuly bílkovin), které jsou v reakci na vliv vnějšího prostředí schopny měnit svou strukturu a předávat buňce příkazy.
Úložný prostor
Proteiny jsou schopny tvořit rezervní usazeniny – v těle zvířat se však bílkoviny zpravidla neukládají. Ale pro každé pravidlo existuje vždy výjimka – to je albumin, který se nachází ve vejcích, a kasein v mléce. Díky proteinům se mohou v těle ukládat například ionty železa, které následně tvoří komplex s proteinem feritinem.
Energie
Bílkoviny se mohou v buňce rozložit na jejich složky, tedy na aminokyseliny. Některé z těchto aminokyselin podléhají štěpení, při kterém se uvolňuje energie. Při odbourání 1 gramu bílkovin se uvolní 17,6 kJ neboli 4,2 kcal energie. Ale proteiny se v této roli používají extrémně zřídka.
Katalytické
Proteiny tzv enzymy, jsou schopny urychlit biochemické reakce probíhající v buňce – to je katalytická funkce proteinů.
Nutriční nebo rezervní
Tuto funkci plní rezervní bílkoviny, které jsou zdrojem výživy pro plod. Takovými bílkovinami mohou být kasein – mléčná bílkovina, ovalbumin – vaječný bílek, prolaminy a gluteliny – rostlinné bílkoviny.
Funkce proti zamrznutí
Nemrznoucí proteiny jsou schopny snížit bod tuhnutí roztoku v buňkách, aby se zabránilo zamrznutí v podmínkách nízké teploty.

Proteiny jako třída organických sloučenin
Nyní se podíváme na proteiny z chemického hlediska. Proteiny v živých organismech obsahují pouze 20 druhů aminokyselin. Všechny z nich jsou alfa aminokyseliny a složení proteinu a pořadí, ve kterém jsou aminokyseliny navzájem spojeny, jsou určeny individuálním genetickým kódem.
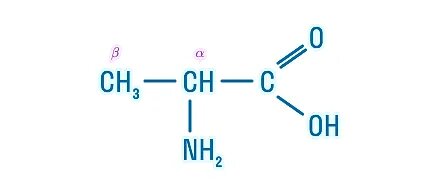
Zde je příklad alfa aminokyseliny, která se nazývá alfa-aminopropan. Ve struktuře aminokyseliny lze rozlišit dvě funkční skupiny: karboxylovou skupinu (—COOH), která je zodpovědná za její kyselé vlastnosti, a aminoskupinu (—NH2), který je zase zodpovědný za základní vlastnosti.
Z toho můžeme usoudit, že všechny aminokyseliny jsou amfoterní sloučeniny a jsou schopny vzájemně reagovat prostřednictvím různých funkčních skupin za vzniku peptidové vazby:
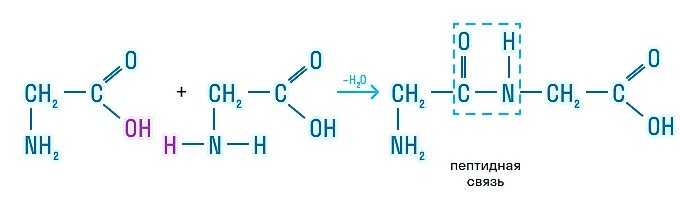
Chemické vlastnosti proteinů jsou velmi omezené. Pojďme se na ně podívat.
Hydrolýza
Všechny proteiny jsou schopné podstoupit hydrolytické reakce. Obecně tato reakce vypadá takto:
Protein + nH2O = směs a-aminokyselin.
Denaturace
Denaturace – je to destrukce sekundární, terciární a kvartérní struktury proteinu bez zničení jeho primární struktury.
Připomeňme si typy proteinových struktur:
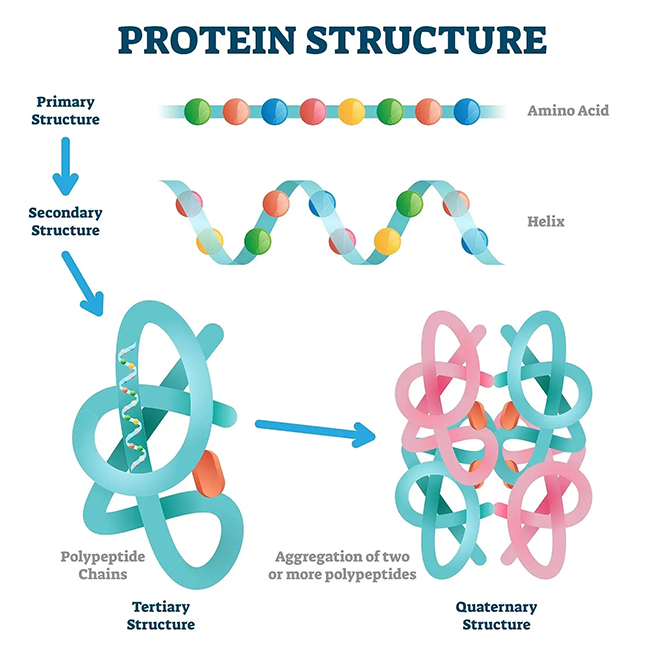
Obrázek je odvozen od „vektorové ilustrace proteinové struktury“ od VectorMine na Shutterstock.
Denaturace může být vratná nebo nevratná:
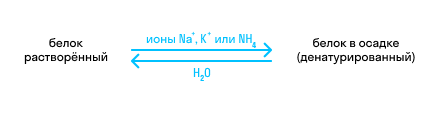
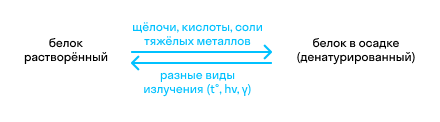
Jak je patrné z podmínek, reverzibilita závisí na reakčních podmínkách. Čím jsou tvrdší, tím je méně pravděpodobné, že bude reakce vratná.
Biuretová reakce (kvalitativní reakce na protein)
Roztok bílkovin + NaOH(10% roztok) + CuSO4 = fialové zbarvení.
Xantoproteinová reakce (kvalitativní reakce na protein)
Roztoky bílkovin žloutnou, když se vaří s koncentrovanou kyselinou dusičnou:
Proteinový roztok + HNO3 (konc) = žluté zbarvení.
Follova reakce (cysteinový test)
Tato reakce je kvalitativní pro aminokyseliny obsahující síru:
Protein + (CH3VRKAT)2Pb + NaOH = PbS + černá barva.

Samotestovací otázky
Která proteinová struktura je nejsilnější?
Kterou z následujících funkcí může vykonávat protein?
Jaká vazba tvoří primární strukturu proteinu?
Když je bílkovina hydrolyzována, je získána (získána).
Aminokyseliny, které tvoří tento protein
Aminokyselina a voda
Protein nepodléhá hydrolýze
Jaká reakce s proteinem vytváří fialovou barvu?
V online kurzech chemie na Skysmartu jsou ještě jasnější příklady funkcí proteinů v buňkách živých organismů. Pomůžeme vám si předmět zamilovat, pochopit nejasná témata, zlepšit známky ve škole a připravit se na státní zkoušky. Vyberte si ten správný kurz a začněte se učit s radostí!
Online škola pro Jednotnou státní zkoušku a Jednotnou státní zkoušku od Skyeng – příprava na klíč na rok s garancí 240+ bodů za 3 předměty Získejte konzultaci




