Otrava digoxinem (digitalis) a její vedlejší účinky
Digoxin je nepochybně nejrozšířenějším přípravkem digitalis ve Spojených státech. Digitoxin je populárnější v Latinské Americe, Evropě a Kanadě. Jeho toxicita se výrazně liší díky jeho nepolární struktuře a z toho vyplývajícím toxicko-kinetickým vlastnostem. Mezi méně používané preparáty digitalisu patří list digitalisu, ouabain, lanatosid C, deslanosid a gitalin. Srdeční glykosidy obsahují tyto rostliny: oleandr obecný (Nerium oleander), digitalis (Digitalis purpurea), konvalinka (Convallaria majalis), oleandr žlutý (Thevetia peruviana) a urginea maritima.
Digoxin je dostupný ve formě tablet po 0,125; 0,25 a 0,5 mg, a také ve formě elixíru – 0,05 mg/ml.
) Toxická dávka. Pokud dítě o hmotnosti 10 kg požije 0,05 mg/kg digoxinu (např. jednu 0,5mg tabletu), očekává se, že koncentrace digoxinu v krvi bude 2 ng/ml nad horní terapeutickou hranicí. I když děti snášejí předávkování digoxinem lépe než dospělí, možnost vážných následků znamená, že jakékoli potenciální nebo domnělé požití léku nad tento limit by mělo vyžadovat dekontaminaci střev a sledování na pohotovosti.
Jakékoli sebevražedné užití léku pacientem pravidelně užívajícím digoxin by mělo být považováno za závažné předávkování. U takových pacientů je obtížné předvídat toxické účinky kvůli řadě faktorů predisponujících k otravě digitalisem.
b) Toxikokinetika. Mezi kinetikou digoxinu a digitoxinu jsou významné rozdíly.
– Sání. Digoxin. Biologická dostupnost závisí na stupni rozpuštění tablet; tento faktor je nyní více standardizován a pohybuje se od 50 do 80 %. Mezi jednotlivé faktory, které způsobují sníženou absorpci, patří současný příjem potravy, malabsorpční syndromy, antacida a snížená gastrointestinální motilita.
Digitoxin. Po perorálním podání je zaznamenána vynikající absorpce. Doba latence po perorálním podání je 1-2 hodiny, s maximální expozicí mezi 4 a 12 hodinami.
– Distribuce:
Digoxin. Digoxin se vyznačuje velkým zdánlivým distribučním objemem (u dospělých 7-8 l/kg; u novorozenců – 10 l/kg; u kojenců – 16 l/kg). Distribuční objem je snížen u onemocnění ledvin, hypotyreózy, během terapie chinidinem a u starších osob (kvůli poklesu svalové hmoty). Počáteční distribuční objem je malý, což může vést k nadměrně vysokým koncentracím ihned po podání. Většina digoxinu je distribuována do kosterního svalstva (přibližně 65 % absorbované dávky). Poměr myokard:plazma je přibližně 30:1.
Digitoxin. Digitoxin je charakterizován vysokým stupněm vazby na proteiny a relativně malým zdánlivým distribučním objemem.
– Vylučování:
Digoxin. 60–80 % digoxinu se vylučuje v nezměněné podobě ledvinami. Terminální poločas je v průměru asi 36 hod. Vylučování žluči a enterohepatální oběh nejsou při terapeutických dávkách významné. Studie ukázaly, že výdej žluči se liší v závislosti na onemocnění jater a metodě odběru vzorků. V závislosti na metodě odběru vzorků se vylučování žluči pohybuje 8 hodin po perorálním podání terapeutické dávky od 30 do 24 %.
Digitoxin. Játra metabolizují digitox odstraněním cukru (digitoxózy) za vzniku epidigitoxigeninu, který se spojí s neaktivním metabolitem. Digoxin je vedlejším produktem metabolismu digitoxinů (asi 8 %). Enterohepatální oběh pravděpodobně odpovídá za dlouhý poločas (asi 100 hodin). Verapamil a diltiazem (ale ne nifedipin) snižují mimorenální clearance v průměru o 29 a 21 %.
– Těhotenství. Poté, co žena v osmém měsíci těhotenství požila 8,9 mg digitoxinu, byly u matky a plodu pozorovány klinické příznaky toxicity digitalisu. Novorozenec zemřel 3 dny po porodu.

c) Drogové interakce. Níže uvedená tabulka shrnuje typy interakcí, které ovlivňují toxikokinetiku digitalisových srdečních glykosidů.
– Erythromycin. Erythromycin inhibuje vývoj Eubacterium lentum, pod jehož vlivem se digoxin ve střevě přeměňuje na své redukční produkty. To může vést ke zvýšení sérových koncentrací digoxinu.
– Erythromycin + tetracyklin. U některých pacientů mohou erytromycin a tetracyklin způsobit zdvojnásobení koncentrací digoxinu, pravděpodobně v důsledku destrukce střevní flóry, která normálně snižuje koncentrace digoxinu a snižuje jeho absorpci.
d) Mechanismus účinku. Obrázek níže schematicky znázorňuje teoreticky předpokládané přímé účinky digitalisu na srdce. Hypomagnezémie může pravděpodobněji než hypokalémie zvýšit toxické účinky digoxinu.

d) Klinický obraz otravy digoxinem. Faktory predisponující k intoxikaci digitalisem jsou uvedeny v tabulce níže. Mortalita je vyšší u pacientů s 5 prognostickými rysy: pokročilý věk, srdeční onemocnění, mužské pohlaví, vysoký stupeň atrioventrikulární blokády a hyperkalémie. Rozdíly mezi akutní a chronickou otravou digoxinem jsou uvedeny v tabulce níže.
– Pravidelné používání. Chronická toxicita digitalisu je často mírná a může být obtížné ji diagnostikovat, protože vedlejší účinky jsou podobné příznakům základního onemocnění.
– Účinky na kardiovaskulární systém. Otrava digitalisem může způsobit jakýkoli typ arytmie. Klasický rytmus toxicity digoxinu je kombinací inhibičních a excitačních účinků (např. neparoxysmální síňová tachykardie s blokádou 2:1). Předčasné ventrikulární extrasystoly jsou nejčastější poruchou rytmu u digitalisové intoxikace, zatímco předčasné síňové a nodální extrasystoly jsou pozorovány méně často. Tyto extrasystoly jsou multifokální nebo bigeminální.
Nejběžnějšími trvalými rytmy jsou junkční únikové rytmy, následované ektopickou síňovou tachykardií s určitým stupněm atrioventrikulární blokády. Regulace rytmu na pozadí ventrikulární fibrilace a podávání digoxinu znamená rozvoj junkčního rytmu v důsledku intoxikace digitalisem. Další intoxikace způsobuje zvýšený nepravidelný rytmus (zvýšený automatismus), nodální tachykardii a Wenckebachovu výstupní blokádu.
Při otravách digitalisem se může vyskytnout atrioventrikulární blok všech stupňů a může být nutná dočasná stimulace. Poruchy rytmu jsou často doprovázeny hypokalémií. Komorová tachykardie a ventrikulární fibrilace patří mezi nejzávažnější arytmie vyvolané digitalisem.
– Nespecifické účinky a účinky na trávicí trakt. Mezi běžné nespecifické a gastrointestinální příznaky intoxikace digitalisem patří malátnost, únava, slabost, anorexie, nauzea, zvracení a bolest hlavy.
– Účinky na vidění. Jsou pozorovány následující poruchy vidění: skotom, rozmazané vidění, fotofobie s barevnou aberací a přechodná slepota.
– Vliv na psychosenzorické mechanismy. Pravidelně jsou hlášeny zmatenost, halucinace a delirium, ale záchvaty jsou vzácné.
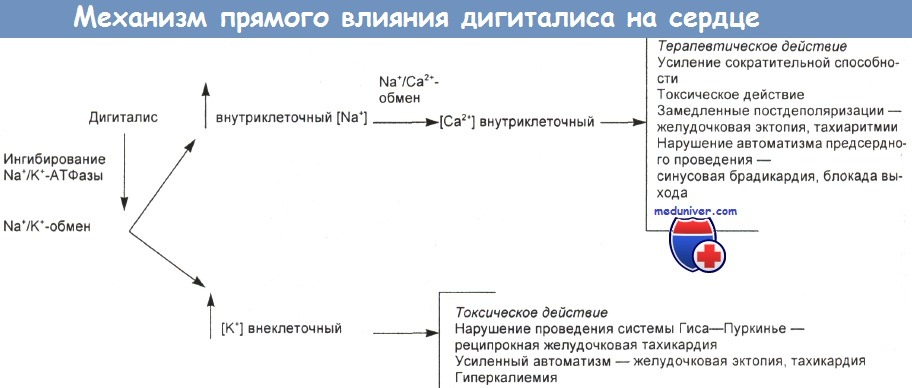
Teoreticky pravděpodobný mechanismus přímého účinku digitalisu na srdce
(e) Nadměrná dávka. Závažné prognostické faktory:
– Věk. Vyšší riziko mají starší pacienti, zejména ti se základním onemocněním. Děti mají často příznivější průběh léčby a snášejí výrazně vyšší maximální koncentrace digoxinu. 18měsíční dítě s maximální koncentrací digoxinu 48 mcg/ml mělo pouze mírné příznaky toxicity digoxinu (koncentrace draslíku v séru 5,2 mEq/l, mírná bradykardie a krátká období junkčního rytmu, sinusové zástavy a atrioventrikulárního bloku) Wenckebach II.
– Hyperkalémie. Mnoho dospělých pacientů s koncentracemi digoxinu 10 ng/ml má koncentrace draslíku přibližně 6 mEq/l.
– Vysoký stupeň atrioventrikulární blokády. Jde o závažný prognostický faktor.
– Plazmatické hladiny digoxinu. Koncentrace vyšší než 15 ng/ml jsou silným prognostickým faktorem.
– Ventrikulární tachykardie. Tento rytmus je spojen s úmrtností 60–65 %.
Klinický obraz. Nevolnost a zvracení jsou nejčastějšími gastrointestinálními projevy otravy digitalisem. Mohou nastat změny duševního stavu. Známky účinků na kardiovaskulární systém jsou typické, jejich projev může být opožděn až o 6 hod. U dětí je pozorována bradykardie a pomalé vedení, ale endogenní kardiostimulátory většinou zajišťují adekvátní propagaci vzruchu a zabraňují hemodynamickým poruchám. Mezi běžné arytmie patří bradykardie (21–75 %), srdeční blok (23–56 %) a tachyarytmie (30–42 %). U dětí jsou ventrikulární arytmie pozorovány méně často.
– Úmrtí. Smrtelné následky při masivním předávkování u dospělých jsou důsledkem exacerbace terapeutických účinků:
• nedostatečnost čerpací funkce srdce v důsledku negativního inotropního účinku (10 % úmrtí);
• porucha vedení s těžkou atrioventrikulární blokádou (20 % úmrtí);
• ventrikulární arytmie způsobené zvýšenou automatikou (70 % úmrtí).

g) Laboratorní nálezy otravy digoxinem:
– Analytické metody. Koncentrace volného digoxinu jsou nejpřesněji měřeny v přítomnosti fragmentu Fab (antigen-vazebná doména) ve více dávkách pomocí ultrafiltrace s fluorescenční polarizační imunoanalýzou. Radioimunoanalýza by se neměla používat k měření sérových koncentrací volného nebo celkového digoxinu, protože poskytne falešné výsledky, pokud jsou ve Fab neobsazená vazebná místa.
– Hladiny digoxinu v séru. Pokles množství K+ iontů v červených krvinkách pod vlivem srdečních glykosidů lze s úspěchem použít jako marker vlivu digitalisu na Na+-, K+-ATPázu. Vymizení iontů K+ z červených krvinek předpovídá závažnost otravy digitalisem; zdá se, že odráží vymizení iontů K+ z myokardiocytů, k čemuž může docházet paralelně s tachyarytmií a poruchami vedení. Klinická užitečnost tohoto markeru musí být potvrzena dalšími studiemi.
– Hladiny digitoxinu v séru. Dospělý pacient, který požil 35 mg digitoxinu, byl léčen fragmenty protilátek Fab (Digitalis antidote BM, 80 mg). Bylo podáno celkem 11 dávek 80 mg Fab fragmentů. Volná frakce sérového digitoxinu byla stanovena pomocí Baxter-Status enzyme-enhanced imunofluorescenčního testu a stanovení celkového digitoxinu bylo provedeno pomocí fluorescenční polarizační imunoanalýzy. Pacient se uzdravil.
8 hodin po odběru mláďat pacient 250 mg digitoxinu Hladina digitoxinu v séru stoupla na 360 mmol/l. Pacientovi byly podány digoxin-specifické Fab fragmenty (Digitalis antidotum BM, 3 mg) ve 1440 dávkách (celkem 480 mg). Sinusový rytmus se stabilizoval a symptomy pacienta ustoupily.
Ukázáno, to digitox-specifické Fab fragmenty monoklonální protilátky lze použít v případech indukované otravy zvířat digitoxinem.
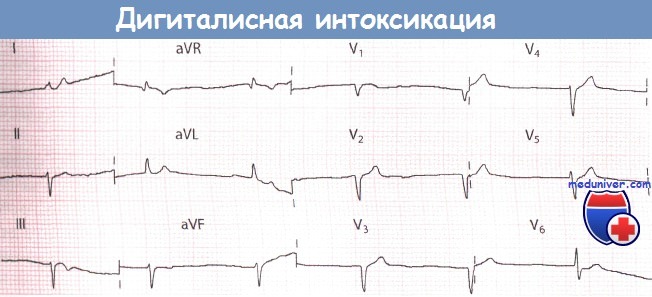
Rytmus z AV junkce u pacienta užívajícího digoxin pro fibrilaci síní (AF).
Obsah digoxinu v krevní plazmě je 5,9 nmol/l.
Video farmakologické, vedlejší účinky inotropů digoxin, dobutamin, milrinon
Střih: Iskander Milevsky. Datum aktualizace publikace: 21.12.2022
Hlavními příčinami rozvoje chronického srdečního selhání (CHF) jsou ischemická choroba srdeční (ICHS), arteriální hypertenze, kardiomyopatie, chlopenní vady, myokarditida atd. Je založena na deficitu kontraktility myofibril, zvýšené rigiditě srdce. svalu, nedostatečná relaxace, která komplexně snižuje jeho prokrvení během diastoly.
Srdeční glykosidy v léčbě srdečního selhání (SS) se používají ke snížení mortality, frekvence hospitalizací, zlepšení kvality života pacienta, zpomalení progrese onemocnění a zvýšení tolerance zátěže.
Klasifikace a názvy léků

Srdeční glykosidy (CG) patří do skupiny kardiotonických (zvyšující kontraktilní aktivitu a zvyšující výkonnost srdce) léků.
Všechny SG jsou látky rostlinného původu. V současné době je identifikováno asi 350 druhů léků s kardiotonickou aktivitou, ale jen několik desítek se používá v medicíně. Syntetické glykosidy se v některých zemích používají pouze v omezené míře.
Klasifikace SG podle původu:
- Léky ze skupiny digitalis (Digitalis):
- Fialová – Digitoxin (v posledních letech se nepoužívá);
- Vlněná – Digoxin, Celanid;
- strophanthin K;
- etrofantin G;
- korglykon;
- tinktura konvalinky;
- Infuze byliny adonis.
Charakteristika SG podle jejich farmakokinetických vlastností:
- Nepolární – lipofilní (Digitoxin). Téměř úplně se adsorbuje v gastrointestinálním traktu, silně se váže na albumin krevní plazmy a podléhá enterohepatální cirkulaci. Mají velmi výrazný kumulativní účinek. Začínají působit během 1,5-2 hodin a jsou vyloučeny z těla za 14-21 dní.
- Středně polární (Digoxin, Celanid). Mají dobrou vstřebatelnost, jsou z 20–30 % vázány na bílkoviny, částečně se biotransformují v játrech a vylučují se stolicí a močí. Může se hromadit v těle. Nástup účinku je po 30-120 minutách (při parenterálním podání – 5-30 minut), úplná eliminace je pozorována po 5-7 dnech.
- Polární (Strophanthin, Korglykon). Špatně se adsorbují v gastrointestinálním traktu (určené hlavně k intravenóznímu podání), nejsou metabolizovány a jsou vylučovány v nezměněné podobě ledvinami. Mají kumulativní (skladovací) schopnosti. Nástup účinku nastává během 5-10 minut, eliminace během 1-3 dnů.
Moderní výzkum ve farmakognozii je zaměřen na vývoj chemických metod přeměny přírodních glykosidů na léčiva se zlepšenými farmakoterapeutickými vlastnostmi, pěstování rostlin s vysokým obsahem SG zemědělskými metodami a hledání nových metod získávání surovin pro léčiva.
Seznam léků ze srdečních glykosidů rostlinného původu:
Také v klinické praxi se používají semisyntetické SG – Methylazid, Acetyldigoxin.
Léky jsou dostupné ve formě tablet nebo v ampulích pro intravenózní podání.
Mechanismus účinku
Srdeční glykosidy jsou komplexní bezdusíkaté sloučeniny rostlinného původu se selektivním kardiotonickým účinkem (schopné zvýšit kontraktilitu myokardu, mrtvici a minutový objem krve bez zvýšení spotřeby kyslíku).
Molekula glykosidu se skládá ze dvou částí:
- Glykon je cukr, který určuje farmakokinetiku léčiva (schopnost rozpouštět se ve vodě, tucích, kyselinách, průchod buněčnou membránou, rychlost absorpce v trávicím traktu, pevnost vazby s plazmatickými proteiny, afinita k receptorům).
- Aglykon je struktura, která je zodpovědná za mechanismus účinku a farmakodynamiku (přímé klinické účinky užívání látky).
Při vstupu do těla SG interagují s receptory nazývanými endodiginy, které se nacházejí v myokardu, kosterních svalech, vláknech hladkého svalstva, játrech, ledvinách a krevních buňkách.
Kardiotonický mechanismus účinku srdečních glykosidů je spojen se schopností:
- inhibovat aktivitu Na-K-ATPázy (enzym odpovědný za činnost sodno-draselné pumpy), čímž se snižuje repolarizace buněk;
- vytváření komplexů s Ca 2+ ionty pro jejich transport uvnitř kardiomyocytu;
- stimulují uvolňování iontů ze sarkoplazmatického retikula do volné cytoplazmy.

V důsledku těchto procesů se zvyšuje koncentrace funkčně aktivního Ca 2+ uvnitř kardiomyocytu. Tento ion zajišťuje neutralizaci troponin-tropomyosinového komplexu a uvolnění aktinového proteinu, který interakcí s myozinem tvoří základ srdeční kontrakce. Ionty Ca 2+ navíc aktivují myosin ATPázu, která dodává kontrakčnímu procesu potřebnou energii.
Vliv iontů Ca 2+ na srdeční činnost:
- Zvýšená síla srdečních kontrakcí;
- Zvýšená srdeční frekvence;
- Zvýšená excitabilita myokardu a automatika kardiostimulátoru.
V důsledku toho se pod vlivem srdečních glykosidů práce srdce stává ekonomičtější, protože optimalizují využití ATP a potřebu kyslíku.
Farmakologické účinky užívání glykosidů:
- Pozitivně inotropní účinek. Síla kontrakcí myokardu se zvyšuje, systola se zkracuje, v důsledku čehož se tepový objem krve a srdeční výdej vrátí do normálu. Částečně kvůli uvolňování katecholaminů a zvýšenému tonusu sympatického nervového systému.
- Negativní chronotropní efekt. Prodloužení diastoly (doba klidu myokardu a plnění koronárních cév krví) a snížení srdeční frekvence.
- Negativní dromotropní účinek. Zpomalení průchodu impulsu převodním systémem srdce (od sinusu do atrioventrikulárního uzlu).
- Diuretické působení. U pacientů s dekompenzovaným srdečním selháním a retencí tekutin v těle se v důsledku zlepšené renální cirkulace a inhibice reabsorpce iontů Na + v distálních tubulech zvyšuje denní diuréza.
- sedativní účinek.
- Zvýšená střevní motilita a tonus žlučníku.
Hemodynamické účinky užívání srdečních glykosidů:
- Posílení a zkrácení trvání systoly;
- Zvýšený minutový objem krve, ejekční frakce levé komory;
- Prodloužení diastoly;
- Snížení srdeční frekvence (účinek na nervus vagus);
- Blíží se normální velikosti srdce;
- Snížení žilního tlaku;
- Optimalizace prokrvení srdečního svalu (zlepšení subendokardiálního průtoku krve, reologické vlastnosti krve);
- Snížený objem cirkulující krve a spotřeba kyslíku myokardem;
- Normalizace tlaku v cévách plicního kruhu, snížení rizika plicního edému, zlepšení výměny plynů, saturace krve kyslíkem;
- Odstranění otoků.
Indikace a kontraindikace
Indikace pro použití SG:

- Akutní a chronické srdeční selhání způsobené poruchou kontraktilní aktivity. (Nejčastěji jsou glykosidy předepisovány pacientům s městnavým CHF funkční třídy II, III nebo IV).
- Fibrilace síní (tachysystolická forma);
- Paroxysmální, supraventrikulární, atriální tachykardie;
- Vegeta-vaskulární kardioneuróza.
Seznam kontraindikací pro použití srdečních glykosidů:
- Těžká bradykardie;
- Atrioventrikulární blok II-III stupně;
- Morgagni-Adams-Stokesův syndrom, WPW;
- Polytopický extrasystol;
- Srdeční selhání s diastolickou dysfunkcí;
- Akutní koronární syndrom;
- Syndrom nemocného sinu (bez zavedeného kardiostimulátoru);
- Infekční myokarditida;
- konstriktivní perikarditida;
- ventrikulární tachykardie;
- Elektrolytová nerovnováha: hypokalémie, hyperkalcémie;
- Stenóza mitrální chlopně;
- Hypertrofická kardiomyopatie (obstrukční forma);
- Aneuryzma hrudní aorty;
- Hypertrofická subaortální stenóza;
- Srdeční tamponáda;
- syndrom karotického sinu;
- restriktivní kardiomyopatie;
- Arytmie způsobené intoxikací glykosidy v anamnéze;
- Chronické selhání ledvin s programem hemodialýzy;
- Přecitlivělost na jakékoli srdeční glykosidy.
Tyto léky vyžadují individuální volbu dávky (u dlouhodobé terapie titruje na 7-10 dní) a pravidelné sledování klinického stavu pacienta (EKG, krevní elektrolyty – K, Ca, Mg).
Pokud je nutné intravenózní podání, dávka léku se rozdělí na 2-3 dávky.
Úprava dávky je nutná u pacientů s:

- Nemoci štítné žlázy. V případě hypotyreózy je třeba snížit dávku srdečních glykosidů. V případě tyreotoxikózy je pozorována relativní rezistence vůči SG.
- Malabsorpční syndrom, krátké střevo. Kvůli zhoršené absorpci léku je nutné zvýšit dávku.
- Závažná respirační patologie (zvýšená citlivost na glykosidy).
- Nerovnováha elektrolytů. Vysoké riziko rozvoje intoxikace digitalisem a arytmie.
U starších pacientů a oslabených pacientů se doba eliminace léku prodlužuje, což zvyšuje riziko nežádoucích účinků a předávkování.
Interakce glykosidů s jinými léčivými látkami vyžadující úpravu dávky:
- Adrenergní agonisté – Epinefrin, selektivní β-agonisté (nekompatibilní, riziko arytmií);
- Aminazin snižuje účinnost SG;
- Anticholinesterázové léky – Prozerin, Physiostigmin (zvyšují bradykardii);
- Glukokortikosteroidy – Hydrokortison, Prednisolon (zvyšují frekvenci nežádoucích účinků);
- Diuretika – Furosemid, Trifas (posilují účinek SG);
- Paracetamol (snížené vylučování glykosidů ledvinami);
- β-blokátory a antagonisté Ca 2+ kanálů (výskyt bradykardie a kompletní srdeční blokády).
Nežádoucí účinky a příznaky předávkování
Během léčby srdečními glykosidy, stejně jako u jiných léků, existuje riziko vzniku nežádoucích účinků:

- Poruchy rytmu a vedení (sinusová bradykardie, blokády, ventrikulární fibrilace);
- Poruchy krevního systému – eozinofilie, trombocytopenie, agranulocytóza;
- Alergické projevy – svědění kůže, hyperémie, vyrážky (erytematózní, papulární), kopřivka, Quinckeho edém.
- Gynekomastie (zvětšení mléčných žláz) u mužů v důsledku estrogenní aktivity SG;
- Duševní poruchy – deprese, sluchové a zrakové halucinace, poruchy paměti, zmatenost;
- Neurologické příznaky – migrény, astenie, vertigo, poruchy spánku, noční můry, apatie nebo nervové vzrušení, myalgie;
- Rozmazané vidění (důsledek retrobulbární neuritidy), fotofobie, efekt záře kolem předmětů, zhoršené vnímání barev (vidět vše ve žlutozelené nebo šedomodré oblasti);
- Nechutenství, bolesti břicha, nevolnost, nedostatečnost viscerálního prokrvení, střevní ischemie.
Při překročení doporučených dávek vykazují SG toxicitu a jsou schopny narušit metabolické procesy a způsobit retenci Ca 2+ v cytoplazmě kvůli problémům s jeho odstraněním z buňky. Zároveň klesá množství ATP, glykogenu, bílkovin, draslíku, hořčíku a metabolismus se přesouvá na anaerobní stranu. Relaxace myokardu v diastole je narušena, tepový objem klesá a zvyšuje se pre- a afterload.
Nedodržení pravidel léčby glykosidy (nezávislé zvýšení dávky nebo zkrácení intervalů mezi dávkami) je spojeno s rozvojem příznaků předávkování:
- Arytmie, bradykardie, AV blokáda, extrasystoly, ventrikulární fibrilace;
- Nevolnost, průjem, nedostatek chuti k jídlu, pocit plného žaludku;
- Bolesti hlavy, vertigo, psychomotorická agitace;
- Snížená zraková ostrost, zhoršené vnímání barev, skotomy (slepé skvrny), zkreslení velikosti předmětu;
- Poruchy vědomí, synkopa.
Léčba příznaků otravy glykosidy
Pokud se objeví příznaky předávkování, musí být přijata následující opatření:
- okamžitě přestat užívat glykosidy;
- Vyvolejte zvracení, opláchněte žaludek;
- Vezměte aktivní uhlí (v poměru 1 tableta na 10 kg hmotnosti) nebo jiný sorbent;
- Okamžitě vyhledejte lékařskou pomoc.
V nemocnici je pacientovi s předávkováním srdečními glykosidy podáván:

- Subkutánní podávání Unithiolu (protijed) 0,05 g na 10 kg hmotnosti 4x denně, cholestyramin;
- Infuze roztoku draslíku (bez inzulínu) nebo kombinovaných léků – Asparkam, Panangin;
- Použití přípravků obsahujících sůl;
- Při bradykardii – podání Atropinu;
- V případě arytmie – intravenózní lidokain, difenin, fentoin, amiodaron;
- V případě silné blokády je instalován umělý kardiostimulátor;
- Vitamínové přípravky – Nikotinamid, Thiamin, Tokoferol, Pyridoxin;
- Léky, které zvyšují metabolismus – Riboxin, Cytochrom C, methyluracil;
- Kyslíková terapie.
Mechanismus účinku Unithiolu (univerzální antidotum) je spojen s vlastností snižovat toxický účinek glykosidů na funkční aktivitu ATPázy a normalizovat energetický metabolismus v myokardu.
Při život ohrožujícím předávkování glykosidy (úmrtnost při intoxikaci dosahuje 40 %) je indikováno podání antidigoxinového séra, Digibindu a imunoglobulinů, které vážou FH. Dialýza a výměnná krevní transfuze jsou neúčinné.
Vzhledem k četnosti nežádoucích účinků, předávkování a jejich souvislosti s porušením režimu srdečních glykosidů by měl lékař zaměřit pozornost pacienta na přísné dodržování předpisů a pacient by si měl před použitím rozhodně prostudovat pokyny k léku. Je přísně zakázáno nezávisle nahradit glykosid analogem bez předchozího souhlasu ošetřujícího lékaře.
Závěry
Glykosidy jsou léky k léčbě chronického srdečního selhání s poruchou kontraktilní funkce. Zvláště dobrý účinek je pozorován u pacientů s kombinací CHF a fibrilace síní. V tomto případě je znázorněno schéma pomalé digitalizace.
Předepisování srdečních glykosidů (nejčastěji Digoxin) pacientům zlepšuje průběh onemocnění, kvalitu života, zvyšuje odolnost vůči fyzické zátěži, aniž by se změnila potřeba kyslíku myokardu. Během užívání SG pacienti pociťují sníženou slabost, dušnost, zlepšení spánku, zmizely otoky a cyanóza, tachykardie se vrátila do normálního rytmu, zvýšila se diuréza a hodnoty EKG se stabilizovaly.









